|
中和热的测定(选修4)<-->酸碱中和滴定中指示剂的选择(选修4)
酸碱中和滴定(选修4)
〖定义〗
用已知物质的量浓度的酸(或碱)测定未知物质的量浓度的碱(或酸)的方法叫中和滴定。
〖原理〗
中和反应中虽然表面上没有明显现象,但pH发生很大变化,在滴定过程中发生pH突变而使指示剂发生颜色变化。通过溶液的颜色变化判断终点,测出酸(或碱)溶液的体积,根据化学方程式中酸碱物质的量之比求出未知溶液的浓度
〖试剂〗
标准液,待测液,指示剂
〖仪器〗
酸式滴定管、碱式滴定管、烧杯、滴定管夹、锥形瓶、铁架台。
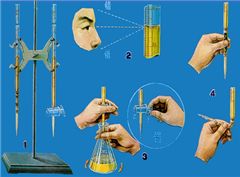

〖步骤〗
①滴定前准备
(1)检查滴定管是否漏液
(2)玻璃仪器洗涤:
a水洗
b用标准液润洗装标准液的滴定管
c用待测液润洗装待测液的滴定管
(3)向用标准液润洗过的滴定管中装入标准液。调整液面到0刻度或0刻度以下(注意零刻度在上方),排除滴定管尖嘴部分气泡,记下刻度读数。
(4)往锥形瓶中加入一定体积(一般为20.00ml)的待测液
注意:锥形瓶只能用蒸馏水洗 ,一定不能用待测液润洗,否则结果会偏高,锥形瓶取液时要用滴定管(或用相应体积规格的移液管),不能用量筒。
(5)向锥形瓶中加入2-3滴指示剂。
②滴定操作
左手操作滴定管,右手摇动锥形瓶,眼睛注意观察锥形瓶中溶液颜色变化,到最后一滴刚好使指示剂颜色发生改变,且半分钟不再变化为止,记下刻度读数。重复上述操作一次或两次。
〖数据处理〗
取两次操作或叁次操作所耗实际试液体积的平均值进行计算。(如果有偏差太大的要舍去)
注意:用滴定管的精确度为0.01ml,故无论用滴定管取待测液或用标准液滴定达终点计数时,待测液和标准液体积都必须精确到小数点后第二位数。
中和热的测定(选修4)<-->酸碱中和滴定中指示剂的选择(选修4)
全网搜索"酸碱中和滴定(选修4)"相关
|

